Aufgaben:
1. Berechne die spezifische Wärmekapazität von
Aluminium aus den ersten drei Versuchsreihen.
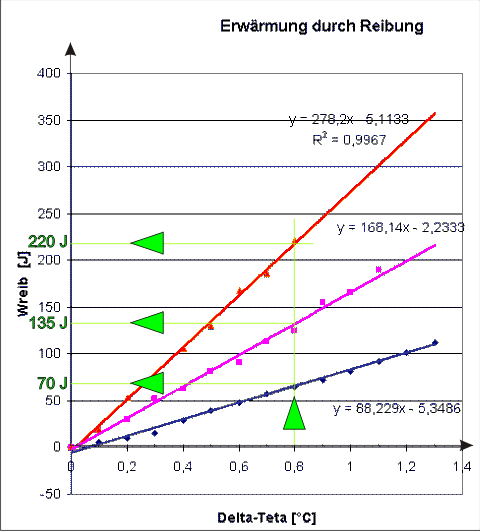 Für eine
beliebige Temperaturdifferenz - hier 0,8 °C - wird für die drei Körper
die zugeführte Arbeit in J aus der Grafik bestimmt (siehe grüne Linien
mit den dicken dreieckigen Pfeilen). Die Massen sind bekannt - 100 g, 200 g
und 300 g. Stelle die Erwärmungsformel nach c um, setze die Werte ein und
rechne aus:
Für eine
beliebige Temperaturdifferenz - hier 0,8 °C - wird für die drei Körper
die zugeführte Arbeit in J aus der Grafik bestimmt (siehe grüne Linien
mit den dicken dreieckigen Pfeilen). Die Massen sind bekannt - 100 g, 200 g
und 300 g. Stelle die Erwärmungsformel nach c um, setze die Werte ein und
rechne aus:
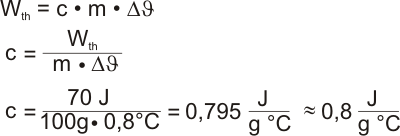
Analog für 200g und 300g Aluminium:
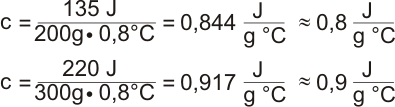
Der Mittelwert aus den drei Messungen ist daher 0,83 J/g °C.
2. Berechne die spezifische Wärmekapazität von Kupfer. Der verwendete Würfel hatte eine Masse m = 244g.
Aus der Grafik liest man wie bei 1. ein Paar für die Temperaturdifferenz und die Wärmearbeit heraus:
Eine Temperaturdifferenz von 1,0°C ergibt sich für ca. 100 J Reibungsarbeit. Der Kupferwürfel hatte 244g.
![]()
3. Leite die Erwärmungsformel aus den Proportionalitätsgleichungen aus der Zusammenfassung zu den Versuchen her.
 Aus
der direkten Proportionalität zwischen Wth und Delta-Theta sowie der Masse
m ergibt sich die Proportionalität aus dem Produkt aus Masse und Temperaturdifferenz.
Die Quotienten aus Wth im Zähler und dem Produkt m mal Delta-Theta im Nenner
sind also alle wertgleich, liefern somit eine Konstante, deren Wert vom Stoff
abhängt.
Aus
der direkten Proportionalität zwischen Wth und Delta-Theta sowie der Masse
m ergibt sich die Proportionalität aus dem Produkt aus Masse und Temperaturdifferenz.
Die Quotienten aus Wth im Zähler und dem Produkt m mal Delta-Theta im Nenner
sind also alle wertgleich, liefern somit eine Konstante, deren Wert vom Stoff
abhängt.
Diese Gleichung wird nach Wth aufgelöst. Das Ergebnis ist die Erwärmungsformel.
c heißt "spezifische Wärmekapazität",
hat die Einheit "J/g °C" und gibt für jeden Stoff an, wieviel
Energie man zuführen muss, um 1 g dieses Stoffes um 1 °C zu erhitzen.
4. Wie funktioniert ein Reed-Kontakt?
In einem REED-Kontakt stehen sich zwei Eisenblechstreifen gegenüber. Wird ein Magnet angenähert, werden die Blechstreifen selbst zu Magneten, deren gegenüberliegende Pole sich gegenseitig anziehen und somit einen elektrischen Kontakt schließen. Beim Entfernen des Magneten öffnet der Schalter wieder, weil die Blechstreifen ihren Magnetismus wieder verlieren.
5. Schau dir die Graphen der Messreihen an und finde dann eine Antwort auf die Frage, ob es sinnvoll ist, die Wegmessung zu verbessern.
Im Vergleich zur sehr genauen Temperaturmessung ist die
Erfassung der Wegstrecken etwas ungenau (+/- ca. 1 m) abhängig davon, wo
beim Umspringen der Temperatur gerade der Magnet für die Rundenzählung
steht. Im Hinblick auf das Gesamtergebnis ist die Genauigkeit dank der vielen
Einzelmessungen ausreichend. Das belegen die Zahlenwerte für c(Aluminium)
und c(Kupfer).
6. Welche Temperatur würde ein Eisenwürfel von 4,0cm Kantenlänge erreichen, wenn er auf der Reibungsscheibe eine durchschnittliche Reibungskraft von 2,30N erfährt und die Scheibe bei obigen Abmessungen unter ihm 265 Umdrehungen macht?
Laut Tabelle ist c(Eisen) = 0,452 J/(g °C). Das Volumen des Würfels ist V = 4cm x 4cm x 4cm = 64cm³. Bei einer Dichte von Eisen von 7,8 g/cm³ ergibt sich eine Masse von m = 7,8 g/cm³ x 64 cm³ = 499 g. DieReibungsarbeit ist W = 2,30 N x 265 m = 609,5 Nm = 610 J. Jetzt liegen alle Daten bereit zum Einsetzen in die umgestellte Erwärmungsformel.
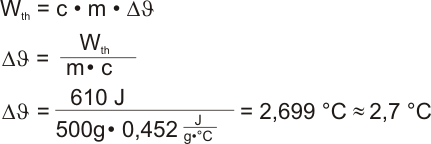
7. Bei Körpern aus Verbundmaterialien kann man nur eine Aussage über deren Wärmekapazität C machen. Welche Einheit hat C? Beschreibe mit eigenen Worten was durch den Wert C angegeben wird. Worin unterscheidet sich C von c?
Besteht ein Körper nicht aus einem einheitlichen Material, kann über die Massenanteile in der Regel keine Aussage gemacht werden. Man kann sich also nicht spezifisch auf einen Stoff beziehen, wohl aber auf die Energie die man pro Grad Celsius Temperaturerhöhung generell aufwenden muss. Genau das wird durch C beschrieben. Die Einheit von C ist J/°C. Handelt es sich beim untersuchten Körper um einen einheitlichen Stoff, kann man sich speziell für diesen Stoff auch noch zusätzlich auf ein Gramm davon beziehen und angeben, welche Energie nötig ist um ein Gramm dieses Stoffes um ein °C in der Temperatur zu erhöhen. Genau das beschreibt die spezifische Wärmekapazität c. Ihre Einheit ist J/(g °C).
8. Wie viel Zink kann man mit 200,0 kJ von 21°C
auf 350K bringen?
c(Zink) = 0,385 J/(g °C); Umrechnung Kelvintemperatur T auf Celsiustemperatur theta:

Die Gleichungen zu den Temperaturpunkten sind um die entsprechenden Einheiten zu ergänzen.
Der Temperatur 350 K entspricht somit die Celsiustemperatur 77 °C. Die
Temperaturdifferenz ist 77° - 21°C = 56°C
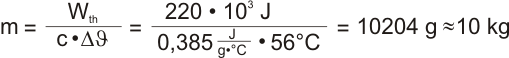
9. Welche Rolle spielt die spezifische Wärmekapazität von Gestein oder Sand im Vergleich zu dem Wert für Wasser für das Klima im Großen (Deutschland oder Europa) und im Kleinen (Regionalklima)?
Dort wo viel Wasser ist, herrscht meist ein ausgeglichenes Klima. Das liegt an der hohen spezifischen Wärmekapazität des Wassers von 4,2 J/(g °C). Gestein und damit auch Sand oder Geröll hat einen viel kleineren Wert etwa um 0,7 bis 0,8 J/(g °C). Bei gleicher Wärmeeinstrahlung von der Sonne (= gleiche Energiemenge) und gleicher Masse dauert es ca. 6 mal so lang bis das Wasser die gleiche Temperatur erreicht wie die Steine in der Nachbarschaft. Steine werden also schneller heiß, kühlen aber auch ebenso schnell wieder aus. Die Temperaturschwankungen sind in trockenen steinigen Gebieten demnach höher als in Gebieten mit viel Wasser.
In wasserreichen Gebieten nimmt das Wasser die Energie von der Sonne langsam auf, kann aber viel davon speichern. Im Winter gibt das Wasser die gespeicherte Energie ebenso langsam wieder ab. Das führt zu einem gemäßigten Klima.
In der Sahara wird es tagsüber sehr heiß, nachts kann die Temperatur
aber auch schnell unter 0°C fallen, weil kein Wasser für den Temperaturausgleich
voehanden ist.
10. Stelle eine Tabelle von c-Werten zusammen, die Stoffe aus deiner Umgebung enthält. Wo kannst du die Werte nachschlagen, wenn sie im Physikbuch nicht zu finden sind?
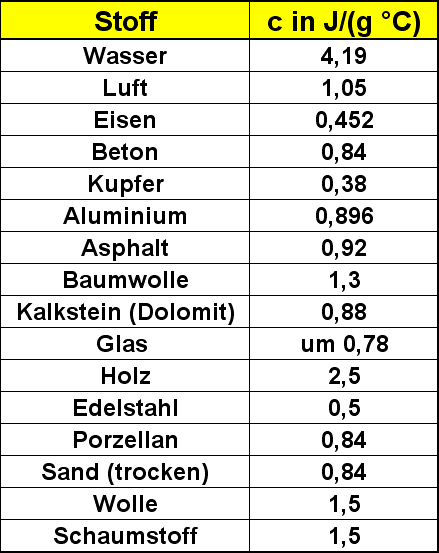
Weitere Werte im WWW z. B. unter: http://ogerstung.de/tabellen/physik.html
oder http://www.wasser-wiki.de/doku.php?id=wasser_eigenschaften:waermekapazitaet:start
Die Suche erfolgte über Google mit den Begriffen "spezifische Wärmekapazität
fester stoffe tabelle".
11. Wenn man mit der Zunge ein -10°C kaltes Eisenstück anleckt, kann die Zunge festfrieren (probier's lieber nicht aus!). Hat dabei die spez. Wärmekapazität oder die Wärmeleitung die Hauptrolle?
Um 1 g Eisen um 1 °C zu erwärmen bedarf es einer relativ geringen Energiemenge. Das ist auf den kleinen c-Wert von 0,452 J/(g °C) zurückzuführen. Die Zunge enthält die alle Muskeln des Menschen einen hohen Wasseranteil und damit eigentlich genügend Energie um ein bisschen Eisen zu erhitzen. Leider ist Eisen ein Metall und damit im Vergleich zu Holz oder Schaumstoff ein recht guter Wärmeleiter, was man von Wasser nicht sagen kann.
Die Energie der Zungenoberfläche (bei feuchten warmen
Handflächen ist es genauso!) wird vom Eisen also sehr schnell weggeleitet
wodurch die Temperatur an der Hautoberfläche rasch unter 0 °C fällt.
Feuchte Hautteile frieren schlagartig an kalten Metalloberflächen fest
und reißen beim Versuch sich zu entfernen ab - autsch!
12. Verschiedene Holzstäbe aus Fichtenholz und
Buchenholz, eine Styroporplatte, ein Pflasterstein und ein Eisenrohr haben die
gleiche Temperatur (50 °C; -18°C). Wie fühlen sich die Gegenstände an? Begründe
deinen Eindruck.
Die Wärmeleitfähigkeit von Stein ist ca. 10 mal so groß wie die von Holz und die wiederum 10 mal so hoch wie die von Schaumstoff. Die c-Werte sind bis auf den von Schaumstoff etwa in der gleichen Größe. Schaumstoff wird demnach an der Kontaktstelle zur Haut sehr rasch die Körpertemperatur annehmen, weil weder (50°C) schnell genug Energie auf der Tiefe des Schaumstoffstücks nachgeliefert werden kann. Schaumstoff hat wegen der geringen Dichte bei vergleichbarem Volumen eine geringe Masse, sodass er insgesamt trotz seines höheren c-Werts wenig Energie speichern kann. Umgekehrt kann der kalte Schaumstoff die von der Hand abgegebene Energie nicht so schnell ins Innere abführen, dass der Körper einen Energieverlust registriert. Heißer Schaumstoff wird daher nicht als heiß und kalter nicht als kalt empfunden.
Bei Holz ist wegen der besseren Wärmeleitfähigkeit dieser Effekt bereits deutlicher zu spüren. Trotzdem passt sich die Holzoberfläche relativ rasch der Handtemperatur an.
Ein 50°C heißer Stein wird dagegen deutlich grenzwertig als heiß empfunden und ein Stein von -18°C als unangenehm kalt. Getoppt wird dieser Eindruck allerdings noch von dickwandigen Metallteilen, vornehmlich aus Kupfer.
13. Weshalb verwendet man als Wärmflasche eine
Gummi- oder Kunststoffhaut und als Füllung heißes Wasser? Warum wird eine Wärmflasche
oft noch in ein Tuch gewickelt?
Heißes Wasser hat im Vergleich zu anderen Stoffen bei gleicher Masse einen hohen Energiegehalt, eignet sich daher als Speichermedium sehr gut. Damit man den Kontakt mit dem heißen Wasser nicht als unangenehm empfindet wird das Wasser in einer Kunststoffhaut verpackt, weil die als schlechter Wärmeleiter die Energieabgabe an die Umgebung drosselt.
Will man den Kontakt mit dem Energieträger noch weiter drosseln, dann verpackt man die Wärmflasche in ein Tuch, welches die Wärmeleitung noch weiter herabsetzt. Das war vor allem früher nötig, weil man sich Mangels Kunststoff einfach einen heißen Ziegelstein oder Wasser in einer Metallflasche als Wärmespender ins Bett gepackt hat.
14. Welche Wärmeenergie liefern die 1,5 L Wasser von 80 °C einer Wärmflasche, bis die Temperatur auf 20°C gefallen ist? Wie würde sich Olivenöl in diesem Fall verhalten?
Temperaturdifferenz: 60 °C
Masse: 1,5 Liter entsprechen 1,5 kg
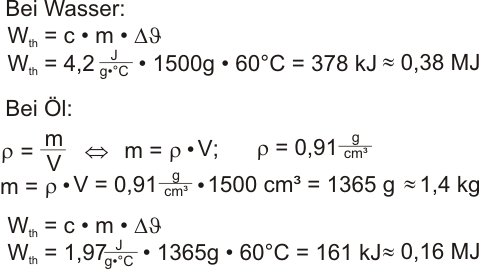
Das Öl würde also weniger als die Hälfte an Energie liefern können. Die Wärmflasche wäre mit Öl gefüllt bereits vor der halben Zeit ausgekühlt wie das bei Wasser der Fall wäre.
(C) Jürgen Grzesina, KRS Neumarkt